No products in the cart.

Neoantigen sebagai Sasaran Rawatan Terapi Kanser Kolorektal
Neoantigen sebagai Sasaran Rawatan Terapi Kanser Kolorektal
Penulis: Profesor Madya Dr. Nadiah Abu¹ & Dr. Nurul Ainaa Adilah Rus Bakarurraini¹
¹UKM Medical Molecular Biology Institute (UMBI),
Universiti Kebangsaan Malaysia
Kanser Kolorektal (CRC) dan Terapi Berasaskan Sel T
Kanser kolorektal (CRC) adalah kanser yang berlaku di kolon dan rektum, iaitu bahagian usus besar. Secara global, CRC merupakan kanser ketiga paling kerap didiagnosis dengan lebih kurang 1.93 juta kes baharu setiap tahun, selepas kanser paru-paru dan payudara. Dalam kalangan lelaki, CRC juga merupakan kanser ketiga paling lazim selepas kanser paru-paru dan prostat.
Selain rawatan tradisional seperti pembedahan dan kemoterapi, terapi berasaskan sel imun semakin mendapat perhatian. Salah satu pendekatan yang sedang berkembang ialah terapi pemindahan sel T (Adoptive T Cell Transfer, ACT). Dalam terapi ini, sel T pesakit dipilih atau diubah suai secara khas sebelum dimasukkan semula ke dalam badan untuk menyerang kanser. Sel T ini boleh diperoleh daripada limfosit penyusup tumor (TIL), sel CAR-T, atau sel T yang direkayasa dengan reseptor TCR. Kebanyakan terapi ini memerlukan antigen yang khusus untuk sel kanser supaya sel T dapat menyerang sel yang betul sahaja.
Apa itu Neoantigen?
Antigen Spesifik Tumor (TSA), atau lebih dikenali sebagai neoantigen, adalah protein unik yang terbentuk akibat mutasi pada DNA sel kanser. Mutasi ini menghasilkan peptida yang tidak normal, yang hanya wujud pada permukaan sel kanser dan tidak ditemui pada sel sihat. Keunikan ini menjadikan neoantigen sasaran yang ideal untuk terapi imun, iaitu rawatan yang menggunakan sistem imun badan untuk menyerang kanser. Kajian menunjukkan bahawa neoantigen boleh merangsang sistem imun dengan berkesan. Contohnya, dalam pesakit leukemia limfosit kronik, neoantigen mampu mencetuskan tindak balas sel T yang berpanjangan. Penyelidikan lain juga menemui neoantigen imunogenik dalam kanser ovari, esofagus, serta kanser kepala dan leher. Malah, para saintis kini sedang membangunkan cara untuk menghasilkan sel T yang dapat mengenali dan menyerang sel kanser berdasarkan neoantigen ini dengan lebih cepat dan tepat.
Biosintesis neoantigen bermula apabila sel kanser menghasilkan peptida abnormal daripada kawasan DNA yang bermutasi. Peptida ini dikenali sebagai DRiPs (Defective Ribosomal Products). Sel kemudian menandakan DRiPs ini dengan protein kecil yang dipanggil ubiquitin, supaya ia dihancurkan oleh mesin pemotong protein dalam sel yang dikenali sebagai proteasom. Proses ini membentuk serpihan peptida pendek. Kebanyakan serpihan ini dipecahkan sepenuhnya, tetapi sebahagian kecil serpihan ini, tetap stabil dan dapat diikat oleh molekul MHC kelas I. Molekul MHC ini bertindak sebagai “papan paparan” yang menunjukkan peptida abnormal ini kepada sel T sitotoksik. Untuk sampai ke papan paparan ini, peptida dibawa ke retikulum endoplasma oleh protein pengangkut TAP dan dibantu oleh protein pendamping seperti calreticulin. Setelah peptida terikat, kompleks MHC-peptida bergerak melalui Golgi dan sampai ke permukaan sel. Di sini, ia mempersembahkan neoantigen kepada sistem imun, yang seterusnya mengaktifkan sel T untuk menyerang sel kanser.
Jenis-jenis Neoantigen
Neoantigen dalam kanser kolorektal (CRC) boleh dikategorikan mengikut jenis mutasi yang menyebabkannya. Antaranya termasuklah:
- SNV (Single Nucleotide Variant) – perubahan satu huruf dalam DNA, yang boleh menghasilkan peptida baru yang dikenali sebagai neoantigen.
- INDEL (Insertion/Deletion) – penambahan atau penghapusan satu atau beberapa huruf dalam DNA, menyebabkan pergeseran bingkai (frameshift) .
- Fusion gene – gabungan dua gen yang biasanya berasingan, menghasilkan protein gabungan yang unik, dan juga boleh menjadi sumber neoantigen.
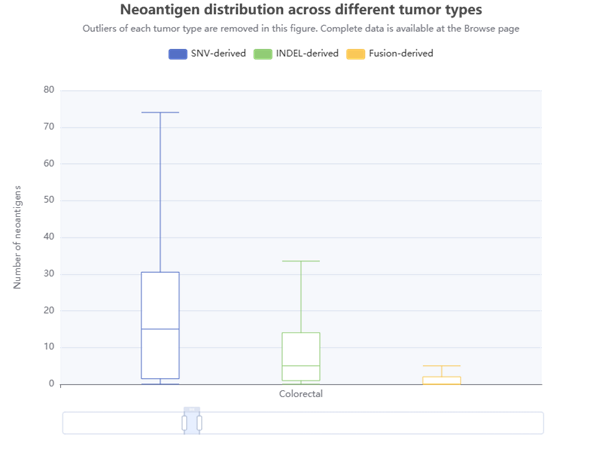
Pelbagai kajian sejak beberapa dekad telah mengenal pasti neoantigen yang berpotensi dijadikan sasaran imunoterapi. Mutasi anjakan bingkai (INDEL) sering menghasilkan kawasan DNA yang sangat berubah, lalu meningkatkan jumlah neoantigen terhasil. Pesakit CRC yang mempunyai tahap Ketidakstabilan Mikrosatelit (MSI) yang tinggi biasanya menghasilkan jumlah neoantigen paling banyak melalui mekanisme ini (Maby et al. 2016). Sebagai contoh, mutasi gen OGT yang berlaku dalam kira-kira 41% kes CRC ber-MSI tinggi menghasilkan neopeptida SLYKFSPFPL yang dapat mencetuskan tindak balas sel T (Ripberger et al. 2003). Kajian Garbe et al pula melaporkan empat neoantigen imunogenik daripada mutasi gen MSH3, iaitu FLLALWECSL, LLALWECSL, IVSRTLLLV dan LIVSRTLLLV (Garbe et al. 2011). Mutasi gen TGFIIβ juga menghasilkan neoantigen RLSSCVPVA yang mampu merangsang tindak balas sel T dalam sel kanser kolon yang mengekspres HLA-A2 (Saeterdal et al.).
Selain INDEL, mutasi nukleotida tunggal (SNV) dalam gen seperti KRAS, TP53 dan BRAF turut menyumbang kepada pembentukan neoantigen. Sebagai contoh, mutasi KRAS kerap berlaku di kodon 12 dan 61 (Dobre et al. 2013). Terdapat juga kejayaan mengasingkan sel T yang menyasarkan mutasi KRAS G12V dan G12D daripada model tikus (Wang et al. 2016). Malah, ujian klinikal fasa I (NCT04117087) sedang menguji keberkesanan vaksin KRAS dalam CRC dan kanser lain. Mutasi gen PIK3CA dan TP53 turut dilaporkan menghasilkan neoantigen dalam kohort CRC yang besar. Kajian ke atas tujuh kohort CRC melaporkan mutasi KRAS G12D (8%), KRAS G12V (5.8%), PIK3CA E545K (3.5%), PIK3CA H1047R (2.5%) dan BMPR2 N583Tfs*44 (Chen et al. 2020).
Walaupun terapi sel T yang menyasarkan neoantigen ini masih di peringkat awal, mutasi-mutasi tersebut dilihat sangat menjanjikan sebagai sasaran imunoterapi pada masa depan. Ujian klinikal tambahan masih diperlukan untuk menilai potensi terapi ini, termasuk gabungannya dengan rawatan standard bagi meningkatkan keberkesanan dalam rawatan CRC.
Catatan:
Prof. Madya Dr. Nadiah Abu merupakan penyelidik biologi molekul dari Institut Biologi Molekul Perubatan (UMBI Universiti Kebangsaan Malaysia yang telah berkecimpung di dalam bidang kanser selama 10 tahun. Kini, beliau sedang menjalankan penyelidikan berkaitan kanser imunologi dalam pesakit kanser kolorektal dan telah memperoleh beberapa geran penyelidikan yang berkaitan dengan kanser imunologi.
Dr. Nurul Ainaa Adilah Rus Bakarurraini – Saintis yang kini bekerja di sebuah syarikat berasaskan imunoterapi di Singapura. Beliau merupakan bekas graduan doktor falsafah dalam bidang Biologi Molekul Perubatan dari Institut Biologi Molekul Perubatan (UMBI) Universiti Kebangsaan Malaysia (UKM).
Rujukan:
- Wu J, Chen W, Zhou Y, Chi Y, Hua X, Wu J, et al. TSNAdb v2.0: the Updated Version of Tumor-specific Neoantigen Database. Genomics Proteomics Bioinforma 2022:in press.
- Rus Bakarurraini, N. A., Ab Mutalib, N. S., Jamal, R., & Abu, N. (2020). The Landscape of Tumor-Specific Antigens in Colorectal Cancer. Vaccines, 8(3), 371. https://doi.org/10.3390/vaccines8030371
- Roudko, V., Bozkus, C. C., Orfanelli, T., Mcclain, C. B., Carr, C., O’donnell, T., Chakraborty, L., Samstein, R., Huang, K. L., Blank, S. V., Greenbaum, B. & Bhardwaj, N. 2020. Shared Immunogenic Poly-Epitope Frameshift Mutations in Microsatellite Unstable Tumors. Cell 183(6): 1634-1649 e1617
- Dobre, M., Comanescu, M., Arsene, D., Iosif, C. & Bussolati, G. 2013. K-Ras Gene Mutation Status in Colorectal Cancer: Comparative Analysis of Pyrosequencing and Pcr-Rflp. Rom J Morphol Embryol 54(3): 567-574.
- Garbe, Y., Maletzki, C. & Linnebacher, M. 2011. An Msi Tumor Specific Frameshift Mutation in a Coding Microsatellite of Msh3 Encodes for Hla-A0201-Restricted Cd8+ Cytotoxic T Cell Epitopes. PLoS One 6(11): e26517
- Maby, P., Galon, J. & Latouche, J. B. 2016. Frameshift Mutations, Neoantigens and Tumor-Specific Cd8(+) T Cells in Microsatellite Unstable Colorectal Cancers. Oncoimmunology 5(5): e1115943.
- Saeterdal, I., Gjertsen Mk Fau – Straten, P., Straten P Fau – Eriksen, J. A., Eriksen Ja Fau – Gaudernack, G. & Gaudernack, G. A Tgf Betarii Frameshift-MutationDerived Ctl Epitope Recognised by Hla-A2-Restricted Cd8+ T Cells. (0340 7004 (Print).
- Wang, Q. J., Yu, Z., Griffith, K., Hanada, K., Restifo, N. P. & Yang, J. C. 2016. Identification of T-Cell Receptors Targeting Kras-Mutated Human Tumors. Cancer Immunol Res 4(3): 204-214.
- Ripberger E, Linnebacher M, Schwitalle Y, Gebert J, von Knebel Doeberitz M. Identification of an HLA-A0201-restricted CTL epitope generated by a tumor-specific frameshift mutation in a coding microsatellite of the OGT gene. J Clin Immunol. 2003;23(5):415-423. doi:10.1023/a:1025329819121
Berikan Komen Anda Di Sini







