No products in the cart.

Antibiotik Tidak Lagi Berkesan? Memahami Ancaman Kerintangan Antimikrob (AMR) Dalam Patogen Penyakit
Antibiotik Tidak Lagi Berkesan? Memahami Ancaman Kerintangan Antimikrob (AMR) Dalam Patogen Penyakit
Penulis: Dr. Nadia Aqilla Shamsusah
Pensyarah Kanan,
Pusat Pengajian Biologi, UiTM Cawangan Negeri Sembilan
Kampus Kuala Pilah
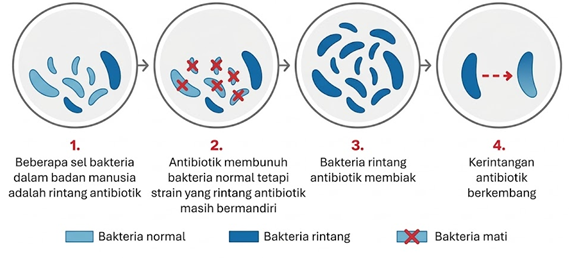
Penggunaan antibiotik sememangnya tidak asing lagi dalam usaha memerangi jangkitan patogen sejak abad ke-20. Selain digunakan untuk merawat penyakit manusia, antibiotik turut digunakan dalam penternakan haiwan dan sektor pertanian di kebanyakan negara membangun (Williams Nguyen et al. 2016). Namun, penggunaan antibiotik secara meluas dan tidak terkawal secara tidak langsung telah mewujudkan satu fenomena yang dikenali sebagai kerintangan antimikrob (antimicrobial resistance, AMR) dalam bakteria. Dalam fenomena ini, walaupun antibiotik dicipta untuk membunuh bakteria, sebahagian bakteria masih mampu bermandiri. Bakteria yang hidup ini akan terus membiak sambil membawa gen kerintangan antibiotik dalam DNA mereka, yang boleh dipindahkan kepada mikroorganisma lain. Hal ini menyebabkan mikroorganisma lain turut menjadi rintang terhadap antibiotik yang digunakan.
Kerintangan antimikrob merupakan salah satu ancaman utama terhadap kesihatan awam dan pembangunan global. Dianggarkan bahawa kerintangan ini menyumbang kepada 1.27 juta kematian di seluruh dunia pada tahun 2019 (Antimicrobial Resistance Collaborators, 2022). Selain menyebabkan kematian dan ketidakupayaan, Bank Dunia menganggarkan bahawa AMR akan meningkatkan kos penjagaan kesihatan sebanyak AS$1 trilion menjelang tahun 2050, serta menyebabkan kerugian keluaran dalam negara kasar (KDNK) global antara AS$1 trilion hingga AS$3.4 trilion setahun menjelang tahun 2030 (Drug-Resistant Infections, 2017). Jangkitan yang disebabkan oleh mikroorganisma yang rintang terhadap antimikrob bukan sahaja sukar dirawat, malah turut meningkatkan risiko berlakunya penyakit yang lebih teruk serta kematian akibat jangkitan tersebut (Salam et al., 2023). Keadaan ini telah membawa kepada suatu epidemik global, di mana banyak antibiotik yang lazim digunakan semakin kurang berkesan dalam merawat jangkitan (Karakonstantis et al., 2017).
Penggunaan antibiotik secara berlebihan, termasuk amalan pengambilan antibiotik sendiri, pemberian antibiotik tanpa preskripsi atau preskripsi berlebihan oleh pengamal perubatan boleh menyebabkan perkembangan kerintangan ubat dalam patogen penyakit. Amalan-amalan ini menggalakkan kelangsungan hidup serta pembiakan bakteria yang rintang terhadap antimikrob (Mancuso et al., 2021). Selain itu, sisa antibiotik dari hospital merupakan salah satu pendorong utama dalam perkembangan serta penyebaran kerintangan antibiotik dalam bakteria kerana mikroorganisma ini mampu bermandiri meskipun melalui proses rawatan kumbahan konvensional sebelum akhirnya dilepaskan ke persekitaran semula jadi (Ashbolt et al., 2013; Chow et al., 2021). Akibatnya, apabila bakteria rintang bertemu dengan bakteria lain di persekitaran, keadaan ini boleh membawa kepada pembentukan dan pembiakan strain bakteria yang lebih bahaya melalui mutasi (UNEP, 2022). Peningkatan suhu global juga dilaporkan menyumbang kepada peningkatan kadar pembiakan bakteria AMR (WHO, 2015).
Beberapa mikroorganisma telah dikenali sebagai “superbug” kerana kerintangan mereka terhadap pelbagai jenis antibiotik. Antara yang terkenal ialah Escherichia coli dan Klebsiella pneumoniae, yang mempunyai kerintangan terhadap antibiotik kelas beta-laktam, menjadikan jangkitan yang disebabkan oleh bakteria ini semakin sukar untuk dirawat (Paterson, 2006; Shaikh et al., 2015). Contoh lain ialah Methicillin-resistant Staphylococcus aureus (MRSA), yang rintang bukan sahaja terhadap antibiotik methicillin, malah juga terhadap antibiotik seperti amoxicillin, oxacillin dan penicillin yang lazim digunakan untuk merawat jangkitan Staphylococcus. Keadaan ini menyebabkan ubat-ubat tersebut tidak lagi berkesan dalam merawat jangkitan MRSA, sekali gus menjadikan jangkitan ini sukar dirawat. Tambahan, fenomena AMR berlaku sangat pantas kerana MRSA pertama kali telah dikenal pasti pada tahun 1961, iaitu setahun selepas antibiotik methicillin diperkenalkan untuk merawat jangkitan S. aureus (Jevons, 1961). Sejak itu, MRSA telah menjadi kebimbangan utama di seluruh dunia kerana kadar kematian yang tinggi berkaitan dengannya (Cuervo et al., 2016). Sehubungan itu, Pseudomonas aeruginosa juga merupakan salah satu patogen utama dalam jangkitan berkaitan penjagaan kesihatan (healthcare-associated infections, HAIs) kerana keupayaannya menentang pelbagai kelas antibiotik. Bakteria ini sering dikaitkan dengan pneumonia yang diperoleh di hospital, jangkitan aliran darah berkaitan kateter serta jangkitan saluran kencing berkaitan kateter. Keupayaan P. aeruginosa untuk membentuk lapisan biofilm dan mengembangkan mekanisme rintangan antibiotik terhadap β-lactam dan aminoglikosida menjadikannya sukar dirawat dan meningkatkan risiko komplikasi serius dalam pesakit.
Oleh itu, beberapa langkah perlu dilaksanakan bagi menangani kerintangan antimikrob daripada terus berkembang. Salah satu pendekatan paling penting ialah penggunaan antibiotik secara berhemah, iaitu hanya mengambil antibiotik atas nasihat doktor dan memastikan ubat dihabiskan mengikut tempoh rawatan yang ditetapkan bagi mengelakkan perkembangan kerintangan dalam bakteria. Inovasi farmaseutikal juga amat penting, termasuk pembangunan antibiotik baharu, terapi kombinasi dan vaksin untuk menentang patogen yang rintang ubat. Selain itu, intervensi terhadap persekitaran seperti peningkatan tahap sanitasi, pengurusan sisa hospital yang betul dan amalan kebersihan yang ketat dapat membantu mengurangkan penyebaran mikroorganisma yang rintang ubat. Kempen kesedaran awam juga memainkan peranan penting dalam mendidik masyarakat tentang bahaya penggunaan antibiotik yang tidak terkawal yang boleh menyumbang secara signifikan kepada peningkatan AMR. Seiring itu, penyelidikan dan inovasi terkini telah menunjukkan potensi dalam mencegah kerintangan antimikrob. Contohnya, saintis giat meneroka sumber semula jadi daripada mikroorganisma bermanfaat, kulat, tumbuhan, haiwan, mineral semula jadi dan sumber makanan lain yang menawarkan pelbagai mekanisme untuk membasmi patogen AMR (Gajić et al., 2025). Terapi faj yang menggunakan virus khusus untuk menjangkiti dan memusnahkan spesies bakteria AMR turut diaplikasikan (Sawa et al., 2024). Selain itu, pembangunan ujian diagnostik pantas membolehkan pihak perubatan mengenal pasti jangkitan dengan segera dan menentukan keperluan antibiotik, sekaligus mengurangkan penggunaan antibiotik yang tidak perlu (Peri et al., 2024).
Kesimpulannya, AMR adalah cabaran kesihatan global yang memerlukan kerjasama menyeluruh antara kerajaan, profesional kesihatan, penyelidik dan masyarakat, serta usaha berterusan dalam penyelidikan, dasar dan pendidikan awam. Hal ini bagi mengelakkan AMR daripada terus merebak sekali gus menjejaskan sektor perubatan, sosial dan ekonomi jika tidak dibanteras dengan kadar segera.
Kredit -Imej janaan AI
Rujukan:
Antimicrobial Resistance Collaborators. (2022). Global burden of bacterial antimicrobial resistance in 2019: A systematic analysis. The Lancet, 399(10325), 629–655. https://doi.org/10.1016/S0140-6736(21)02724-0
Ashbolt, N. J., Amézquita, A., Backhaus, T., Borriello, P., Brandt, K. K., Collignon, P., Coors, A., Finley, R., Gaze, W. H., Heberer, T., et al. (2013). Human health risk assessment (HHRA) for environmental development and transfer of antibiotic resistance. Environmental Health Perspectives, 121(9), 993–1001.
Chow, L. K. M., Ghaly, T. M., & Gillings, M. R. (2021). A survey of sub-inhibitory concentrations of antibiotics in the environment. Journal of Environmental Sciences, 99, 21–27.
Cuervo, G., Gasch, O., Shaw, E., Camoez, M., Domínguez, M. Á., Padilla, B., Pintado, V., Almirante, B., Lepe, J. A., López-Medrano, F., Ruiz de Gopegui, E., Martínez, J. A., Montejo, J. M., Perez-Nadales, E., Arnáiz, A., Goenaga, M. Á., Benito, N., Horcajada, J. P., Rodríguez-Baño, J., Pujol, M., … REIPI/GEIH study group (2016). Clinical characteristics, treatment and outcomes of MRSA bacteraemia in the elderly. The Journal of infection, 72(3), 309–316. https://doi.org/10.1016/j.jinf.2015.12.009
Gajić, I., Kekić, D., Janković, M., Tomić, N., Skoric, M., Petrovic, M., Ćulafić, D., Opavski, N., Ristivojević, P., Ristivojević, M., & Luković, B. (2025). Nature’s arsenal: Uncovering antibacterial agents against antimicrobial resistance. Antibiotics, 14(3). https://doi.org/10.3390/antibiotics14030253
Henly, H. (2026). Antimicrobial resistance (AMR) — A global burden, an individual problem. RGA. https://www.rgare.com/knowledge-center/article/antimicrobial-resistance-%28amr%29—a-global-burden-an-individual-problem
Jevons, M. P. (1961). “Celbenin”-resistant staphylococci. BMJ, 1, 124–125.
Karakonstantis, S., & Kalemaki, D. (2019). Antimicrobial overuse and misuse in the community in Greece and link to antimicrobial resistance using methicillin-resistant S. aureus as an example. Journal of Infection and Public Health, 12(4), 460–464. https://doi.org/10.1016/j.jiph.2019.03.017
Mancuso, G., Midiri, A., Gerace, E., & Biondo, C. (2021). Bacterial antibiotic resistance: The most critical pathogens. Pathogens, 10(10), 1310. https://doi.org/10.3390/pathogens10101310
Paterson, D. L. (2006). Resistance in gram-negative bacteria: Enterobacteriaceae. American Journal of Infection Control, 34(5 Suppl.), 20–28. https://doi.org/10.1016/j.ajic.2006.05.238
Peri, A., Chatfield, M., Ling, W., Furuya-Kanamori, L., Harris, P., & Paterson, D. (2024). Rapid diagnostic tests and antimicrobial stewardship programs for the management of bloodstream infection: What is their relative contribution to improving clinical outcomes? A systematic review and network meta-analysis. Clinical Infectious Diseases, 79, 502–515. https://doi.org/10.1093/cid/ciae234
Salam, M. A., Al-Amin, M. Y., Salam, M. T., Pawar, J. S., Akhter, N., Rabaan, A. A., & Alqumber, M. A. A. (2023). Antimicrobial resistance: A growing serious threat for global public health. Healthcare (Basel, Switzerland), 11(13), 1946. https://doi.org/10.3390/healthcare11131946
Sawa, T., Moriyama, K., & Kinoshita, M. (2024). Current status of bacteriophage therapy for severe bacterial infections. Journal of Intensive Care, 12, Article 7. https://doi.org/10.1186/s40560-024-00759-7
Shaikh, S., Fatima, J., Shakil, S., Rizvi, S. M. D., & Kamal, M. A. (2015). Antibiotic resistance and extended spectrum beta-lactamases: Types, epidemiology and treatment. Saudi Journal of Biological Sciences, 22(1), 90–101. https://doi.org/10.1016/j.sjbs.2014.08.002
Williams-Nguyen, J., Sallach, J. B., Bartelt-Hunt, S., Boxall, A. B., Durso, L. M., McLain, J. E., Singer, R. S., Snow, D. D., & Zilles, J. L. (2016). Antibiotics and antibiotic resistance in agroecosystems: State of the science. Journal of Environmental Quality, 45(2), 394–406. https://doi.org/10.2134/jeq2015.07.0336
World Bank. (2017, March). Drug-resistant infections: A threat to our economic future. https://www.worldbank.org/en/topic/health/publication/drug-resistant-infections-a-threat-to-our-economic-future
United Nations Environment Programme (UNEP). (2022). Antimicrobial resistance: A global threat. https://www.unep.org/resources/report/antimicrobial-resistance-global-threat
World Health Organization (WHO). (2015). Global action plan on antimicrobial resistance. https://www.who.int/publications/i/item/9789241509763
Berikan Komen Anda Di Sini